En elektrisk strömkälla är en anordning med vilken en elektrisk ström skapas i en sluten elektrisk krets. För närvarande har ett stort antal typer av sådana källor uppfunnits. Varje typ används för specifika ändamål.
Innehåll
Typer av elektriska strömkällor
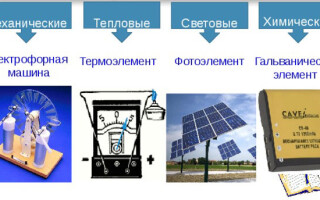
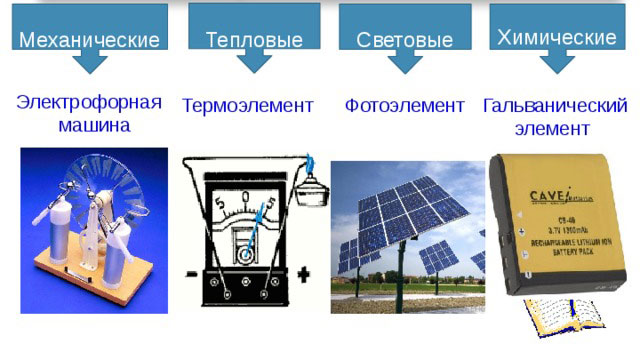
Det finns följande typer av elektriska strömkällor:
- mekanisk;
- termisk;
- ljus;
- kemisk.
Mekaniska källor
Dessa källor omvandlar mekanisk energi till elektrisk energi. Omvandlingen utförs i speciella enheter - generatorer. Huvudgeneratorerna är turbogeneratorer, där den elektriska maskinen drivs av ett gas- eller ångflöde, och hydrogeneratorer, som omvandlar energin från fallande vatten till elektricitet. Det mesta av elektriciteten på jorden produceras just av mekaniska omvandlare.

Värmekällor
Här omvandlas värmeenergi till elektricitet. Förekomsten av en elektrisk ström beror på temperaturskillnaden mellan två par kontaktande metaller eller halvledare - termoelement. I detta fall överförs laddade partiklar från ett uppvärmt område till ett kallt. Strömmens storlek beror direkt på temperaturskillnaden: ju större skillnaden är, desto större blir den elektriska strömmen. Halvledarbaserade termoelement ger en termoelektrisk effekt 1000 gånger större än bimetalliska, så strömkällor kan göras från dem. Metalltermoelement används endast för att mäta temperatur.

REFERENS! För att få ett termoelement måste du koppla ihop 2 olika metaller.
För närvarande har nya grundämnen utvecklats baserat på omvandlingen av värme som frigörs under det naturliga sönderfallet av radioaktiva isotoper. Sådana element kallas radioisotop termoelektrisk generator. I rymdfarkoster har en generator som använder isotopen plutonium-238 visat sig väl. Den ger en effekt på 470 W vid en spänning på 30 V. Eftersom halveringstiden för denna isotop är 87,7 år är generatorns livslängd mycket lång. Ett bimetalltermoelement används för att omvandla värme till elektricitet.
Ljuskällor
Med utvecklingen av halvledarfysik i slutet av 1900-talet uppträdde nya strömkällor - solbatterier, där ljusenergi omvandlas till elektrisk energi. De använder egenskapen hos halvledare för att producera spänning när de utsätts för ett ljusflöde. Denna effekt är särskilt stark i kiselhalvledare. Men ändå överstiger inte effektiviteten av sådana element 15%.Solpaneler har blivit oumbärliga i rymdindustrin, och har börjat användas i vardagen. Priset på sådana nätaggregat minskar ständigt, men förblir ganska högt: cirka 100 rubel per 1 watt effekt.

Kemiska källor
Alla kemiska källor kan delas in i 3 grupper:
- Galvanisk
- Batterier
- Termisk
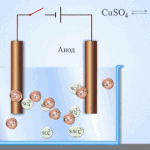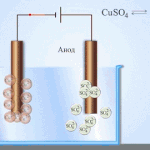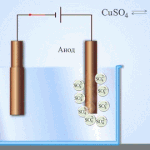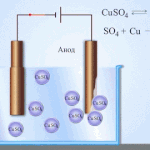
Galvaniska celler fungerar på basis av växelverkan mellan två olika metaller placerade i en elektrolyt. Olika kemiska grundämnen och deras föreningar kan fungera som par av metaller och en elektrolyt. Elementets typ och egenskaper beror på detta.
VIKTIG! Galvaniska celler används endast en gång, d.v.s. När de väl har tömts kan de inte återställas.
Det finns 3 typer av galvaniska källor (eller batterier):
- Salt;
- Alkalisk;
- Litium.
Salta, eller på annat sätt "torra", batterier använder en pastaliknande elektrolyt från ett salt av en metall, placerad i en zinkkopp. Katoden är en grafit-manganstav placerad i mitten av koppen. Billiga material och enkel tillverkning av sådana batterier gjorde dem till de billigaste av alla. Men när det gäller egenskaper är de betydligt sämre än alkaliska och litium.

Alkaliska batterier använder en pastaaktig lösning av alkali, kaliumhydroxid, som elektrolyt. Zinkanoden ersattes med zinkpulver, vilket gjorde det möjligt att öka strömuttaget med elementet och driftstiden. Dessa element tjänar 1,5 gånger längre än salt.
I en litiumcell är anoden gjord av litium, en alkalimetall, vilket avsevärt ökade drifttiden. Men samtidigt ökade priset på grund av den relativt höga kostnaden för litium. Dessutom kan ett litiumbatteri ha en annan spänning beroende på katodmaterialet.De producerar batterier med en spänning på 1,5 V till 3,7 V.
Batterier är källor till elektrisk ström som kan utsättas för många laddnings-urladdningscykler. Huvudtyperna av batterier är:
- Bly-syra;
- litiumjon;
- Nickel-kadmium.
Blysyrabatterier består av blyplattor nedsänkta i en lösning av svavelsyra. När en extern elektrisk krets är sluten uppstår en kemisk reaktion, som ett resultat av vilken bly omvandlas till blysulfat vid katoden och anoden, och vatten bildas också. Under laddning reduceras blysulfat vid anoden till bly och vid katoden till blydioxid.

REFERENS! Ett element i ett bly-zink batteri genererar en spänning på 2 V. Genom att seriekoppla elementen kan du få vilken spänning som helst som är en multipel av 2. Till exempel i bilbatterier är spänningen 12 V, eftersom. kopplade 6 element.
Litiumjonbatteriet har fått sitt namn från det faktum att litiumjoner fungerar som bärare av elektricitet i elektrolyten. Jonerna har sitt ursprung vid katoden, som är gjord av litiumsalt på ett aluminiumfoliesubstrat. Anoden är gjord av olika material: grafit, koboltoxider och andra föreningar på ett kopparfoliesubstrat.
Spänningen, beroende på de komponenter som används, kan vara från 3 V till 4,2 V. På grund av den låga självurladdningen och ett stort antal laddnings-urladdningscykler har litiumjonbatterier blivit mycket populära i hushållsapparater.
VIKTIG! Litiumjonbatterier är mycket känsliga för överladdning.Därför, för att ladda dem, måste du använda laddare avsedda endast för dem, som har inbyggda speciella kretsar som förhindrar överladdning. Annars kan batteriet förstöras och antändas.

I nickel-kadmium-batterier är katoden gjord av nickelsalt på ett stålnät, anoden är gjord av kadmiumsalt på ett stålnät, och elektrolyten är en blandning av litiumhydroxid och kaliumhydroxid. Den nominella spänningen för ett sådant batteri är 1,37 V. Det tål från 100 till 900 laddnings-urladdningscykler.
REFERENS! Nickel-kadmium-batterier kan förvaras i urladdat tillstånd, till skillnad från litiumjon.
Termiska kemiska element fungerar som reservkraftkällor. De ger utmärkta egenskaper när det gäller specifik strömtäthet, men har en kort livslängd (upp till 1 timme). De används främst inom raketteknik, där tillförlitlighet och kortvarig drift behövs.
VIKTIG! Inledningsvis kan termiska kemiska källor inte producera en elektrisk ström. I dem finns elektrolyten i ett fast tillstånd, och för att få batteriet i fungerande skick är uppvärmning till 500-600 ° C nödvändig. Sådan uppvärmning utförs av en speciell pyroteknisk blandning, som antänds vid rätt tidpunkt.
Skillnaden mellan en verklig källa och en idealisk
En ideal källa, enligt fysikens lagar, måste ha oändlig intern resistans för att säkerställa en konstant elektrisk ström i lasten. Verkliga källor har ett ändligt inre motstånd, vilket innebär att strömmen beror på både den externa belastningen och den inre resistansen.
Här är en kort sammanfattning av olika moderna källor för elektrisk ström. Som framgår av recensionen har hittills ett imponerande antal källor skapats med egenskaper som lämpar sig för alla tillämpningar.
Liknande artiklar: